Cho 8,4 gam sắt tác dụng với lượng HCl vừa đủ. Dẫn toàn bộ lượng khí sinh ra qua 16g đồng ( II ) oxit nung nóng
a, Tính thể tích khí hidro sinh ra ( đktc )
b, Tính lượng kim loại đồng thu được sau phản ứng
giúp mình với !!!


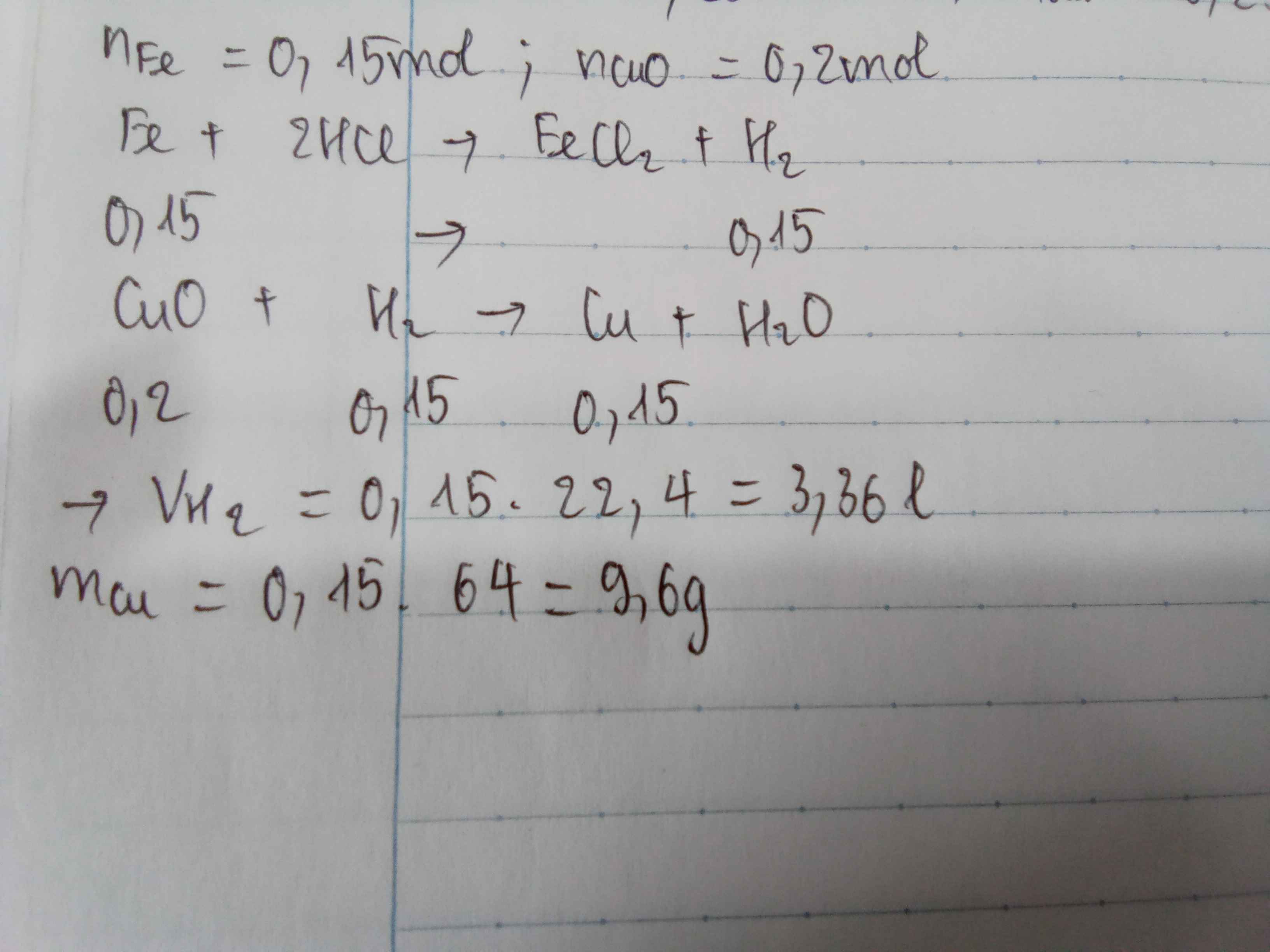


Mik làm rồi nhé
Bn vuối xuống dưới là thấy